David Noncent et Petit Noël Lafleur
Équipe de Recherche sur les Changements Climatiques (ERC2), Université Quisqueya, Port-au-Prince, Haïti
Ecole Normale Supérieure, Université d’Etat d’Haïti, Port-au-Prince, Haïti
Executive summary
Malgré sa reconnaissance comme aire protégée d’importance nationale, le Parc National Naturel Lagon des Huîtres (PNN-LdH), situé dans le département du Sud-Est d’Haïti, ne disposait d’aucun inventaire floristique systématique, ni d’herbier de référence. Dans le cadre du Projet INOVEE (Initiative pour la Nature et l’Optimisation des Valeurs Écologiques et Économiques), un inventaire botanique a été réalisé dans les principaux écosystèmes du parc (forêts sèches xérophytiques, mangroves, dunes côtières et zones de transition), combiné à la création d’un herbier de référence. Au total, 71 espèces végétales vasculaires réparties dans 30 familles botaniques ont été recensées. Les Fabaceae dominent l’inventaire (10 espèces, 14,1 %), suivies des Lamiaceae (4 espèces), des Cactaceae, Apocynaceae et Myrtaceae (3 espèces chacune). Deux espèces endémiques d’Hispaniola ont été documentées (Allophylus haitiensis and Malpighia hispaniolica), ainsi que des espèces menacées dont Guaiacum officinale (classé « En danger » par l’UICN). Environ 77 % des espèces recensées présentent un usage médicinal traditionnel documenté, témoignant de l’importance ethnobotanique de cette flore. L’herbier constitué représente le premier outil de documentation botanique systématique pour le PNN-LdH et servira de référence pour le suivi de la biodiversité et les stratégies de conservation futures.
Keywords: biodiversité végétale, herbier, forêt sèche, mangrove, xérophyte, ethnobotanique, aire protégée, Haïti, Hispaniola
Abstract
Despite its recognition as a nationally important protected area, the Lagon des Huîtres National Nature Park (PNN-LdH) in southeastern Haiti lacked any systematic floristic inventory or reference herbarium. As part of the INOVEE Project (Initiative for Nature and Optimization of Ecological and Economic Values), a botanical inventory was conducted across the park’s main ecosystems (xerophytic dry forests, mangroves, coastal dunes, and transitional zones), combined with the creation of a reference herbarium. A total of 71 vascular plant species belonging to 30 botanical families were recorded. Fabaceae dominated the inventory (10 species, 14.1%), followed by Lamiaceae (4 species), Cactaceae, Apocynaceae, and Myrtaceae (3 species each). Two Hispaniolan endemics were documented (Allophylus haitiensis and Malpighia hispaniolica), along with threatened species including Guaiacum officinale (listed as Endangered by the IUCN). Approximately 77% of the species recorded have documented traditional medicinal uses, reflecting the ethnobotanical significance of this flora. The herbarium constitutes the first systematic botanical documentation tool for the PNN-LdH and will serve as a baseline for biodiversity monitoring and future conservation strategies.
Keywords: plant biodiversity, herbarium, dry forest, mangrove, xerophyte, ethnobotany, protected area, Haiti, Hispaniola
1. Introduction
La biodiversité végétale dans les régions tropicales constitue le socle des équilibres écosystémiques mondiaux, fournissant des services fondamentaux : régulation climatique, protection contre l’érosion, ressources alimentaires et médicinales, et séquestration du carbone (Ward et al., 2016). La Caraïbe est reconnue comme l’un des principaux hotspots de biodiversité mondiale, avec un taux d’endémisme végétal dépassant 34 % (Myers et al., 2000). Cette richesse biologique est aujourd’hui soumise à une pression sans précédent : le rythme de disparition des espèces est estimé de 100 à 1 000 fois supérieur au taux naturel d’extinction (Ceballos et al., 2017).
Les herbiers botaniques représentent un outil scientifique irremplaçable pour la conservation. Davis et al. (2023), dans Trends in Ecology & Evolution, soulignent que ces collections sont passées d’archives statiques à des outils dynamiques pour la biologie de la conservation, avec plus de 350 millions de spécimens conservés dans environ 3 000 herbiers mondiaux. Lang et al. (2018) démontrent que les herbaria permettent de tracer les décalages phénologiques sur des décennies, une information inaccessible par d’autres méthodes dans les pays tropicaux à faibles données historiques. Meineke et al. (2018) confirment le potentiel sous-exploité de ces collections pour la détection de changements phénologiques en réponse au réchauffement climatique.
Haïti, partageant l’île d’Hispaniola avec la République dominicaine, est un hotspot de biodiversité caraïbéenne avec plus de 5 000 espèces végétales dont 36 % endémiques (Haiti Biodiversity, 2023). Cependant, la déforestation massive – le couvert forestier est estimé à seulement 3 % du territoire, contre 60 % au début du XXᵉ siècle (FAO, 2010) – exacerbée par la pauvreté et les catastrophes naturelles, menace gravement ces écosystèmes. Hong et al. (2025), utilisant des séries temporelles Landsat, documentent une perte forestière de l’ordre de 1 %/an en Haïti, révélant un contraste saisissant avec la République dominicaine. Cano-Ortiz et al. (2016) identifient Hispaniola comme un centre d’endémisme de premier ordre avec 6 000 espèces végétales dont 34 % uniques.
Le Parc National Naturel Lagon des Huîtres (PNN-LdH), couvrant 9 640,60 hectares dans la commune de Belle-Anse, a été officiellement déclaré aire protégée en 2017. Il fait partie des quatre unités de conservation du Massif de la Selle, classé Réserve de la Biosphère. Cependant, le parc fait face à des pressions anthropiques persistantes : coupe illégale de bois, surpêche, érosion côtière, élevage caprin non contrôlé, et à une insécurité alimentaire classée au niveau IPC 4 (Noncent & Lafleur, 2025a).
Malgré la reconnaissance du PNN-LdH comme zone de haute valeur écologique, les données scientifiques disponibles sur sa flore restent fragmentaires. Hilaire (2014) et TNC (2019) ont fourni des évaluations écologiques générales, mais aucun inventaire floristique systématique accompagné de la création d’un herbier de référence n’avait encore été réalisé. L’objectif principal est de documenter la biodiversité végétale du PNN-LdH via un inventaire exhaustif et la création d’un herbier institutionnel, en analysant ses implications pour la conservation, l’écotourisme et le développement durable, dans le cadre des ODD 14 et 15 de l’Agenda 2030.
2. Zone d’étude et méthodologie
2.1. Présentation de la zone d’étude
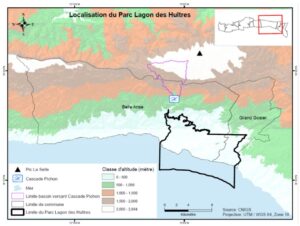
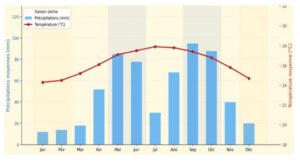
Le PNN-LdH est situé dans le département du Sud-Est d’Haïti (Figure 1), couvrant trois sections communales des communes de Belle-Anse et Grand-Gosier. Ses coordonnées géographiques (UTM WGS84, zone 18N) s’étendent entre 813 337,84 et 827 305,01 m E et entre 2 000 099,90 et 2 023 125,67 m N. Le parc protège 6 061 hectares de forêts sèches côtières et de milieux humides, ainsi que 3 596 hectares d’écosystèmes marins, incluant mangroves, lagunes côtières, estuaires et deltas (TNC, 2019). Il est situé entre le niveau de la mer et 450 m d’altitude, avec un climat tropical subhumide semi-aride. Les précipitations annuelles moyennes varient entre 605 et 650 mm, avec deux saisons pluvieuses (avril–juin et août–octobre) et deux saisons sèches (décembre–mars et mi-juin à mi-juillet). La température annuelle moyenne est de 26,1 °C (Figure 2 ; Céliscar, 2017).
2.2. Matériels et méthodes
L’étude s’est déroulée de mars à septembre 2025. Une équipe pluridisciplinaire (botaniste, éducateurs, collecteurs communautaires) a prospecté les zones représentatives des principaux habitats du parc, en privilégiant les écosystèmes de mangroves (Rhizophora mangle, Laguncularia racemosa, Avicennia germinans) et de forêts sèches xérophytiques (Planche 1). L’inventaire floristique a été réalisé selon la méthode de relevés phytosociologiques de Braun-Blanquet, adaptée aux conditions locales.

L’identification des spécimens a été réalisée par confrontation avec les ouvrages de référence (Liogier, 1982–2000 ; Alain, 1953–1979) et les bases de données taxonomiques Tropicos (Missouri Botanical Garden) et The Plant List. Pour chaque point de collecte, les coordonnées GPS (UTM WGS84, zone 18N ; précision ±5 m), le type d’habitat, la date, le nom vernaculaire créole et les observations morphologiques ont été systématiquement enregistrés (Planche 2). Des entretiens semi-directifs avec 20 informateurs locaux (agriculteurs, guérisseurs, pêcheurs) ont permis de documenter les usages ethnobotaniques.

2.3. Préparation de l’herbier
Les spécimens, privilégiant les individus en fleurs ou en fruits, ont été pressés entre des feuilles de papier journal absorbant, changé quotidiennement pendant les trois premiers jours, puis séchés pendant 7 à 14 jours. Les spécimens séchés ont été montés sur des planches cartonnées A3 (420 × 297 mm), accompagnés de fiches scientifiques détaillées (16 champs d’information). Les étiquettes ont été rédigées à l’encre noire indélébile sur papier de qualité archive. La conservation se fait à température ambiante, à faible humidité relative et à l’abri de la lumière directe.
2.4. Limites méthodologiques
L’inventaire n’a pas été structuré selon un plan d’échantillonnage statistique strict (transects systématiques, quadrats permanents). Les zones prospectées ont été sélectionnées sur la base de l’accessibilité et de la représentativité des principaux types d’habitats. Le nombre réel d’espèces est vraisemblablement supérieur aux 71 documentées. La taille de l’échantillon ethnobotanique (20 informateurs) est relativement modeste.
3. Résultats
3.1. Richesse spécifique et composition taxonomique
L’inventaire a permis de recenser 71 espèces végétales vasculaires réparties dans 30 familles botaniques (Figure 3, Tableau 1). Les Fabaceae (sensu lato) dominent avec 10 espèces (14,1 %), suivies des Lamiaceae (4 espèces, 5,6 %), puis des Cactaceae, Apocynaceae et Myrtaceae (3 espèces chacune, 4,2 %).
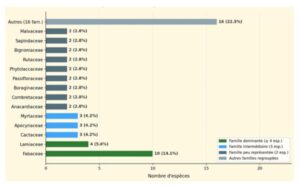
Tableau 1. Synthèse des familles botaniques recensées au PNN-LdH (Nb esp. = nombre d’espèces ; % = pourcentage du total ; End. = espèces endémiques ; Médic. = espèces à usage médicinal documenté).
| Famille botanique | Nb esp. | % total | End. | Médic. | Principales espèces |
| Fabaceae (s.l.) | 10 | 14,1 | 0 | 8 | Prosopis juliflora, Vachellia farnesiana… |
| Lamiaceae | 4 | 5,6 | 0 | 4 | Clerodendrum sepium, Ocimum gratissimum… |
| Cactaceae | 3 | 4,2 | 0 | 2 | Opuntia ficus-indica, Pilosocereus polygonus… |
| Apocynaceae | 3 | 4,2 | 0 | 3 | Calotropis gigantea, Angadenia berteroi… |
| Myrtaceae | 3 | 4,2 | 0 | 3 | Psidium guajava, Syzygium cumini… |
| Sapindaceae | 2 | 2,8 | 1 | 2 | Dodonaea viscosa, Allophylus haitiensis* |
| Zygophyllaceae | 1 | 1,4 | 0 | 1 | Guaiacum officinale** (UICN VU, CITES II) |
| Zamiaceae | 1 | 1,4 | 1 | 0 | Zamia rosea* (endémique rare) |
| Autres (16 fam.) | 14 | 19,7 | 0 | 12 | Moraceae, Polygonaceae, Malpighiaceae… |
| TOTAL | 71 | 100 | 2 | 55 (77 %) |
* Espèce endémique d’Hispaniola. ** Espèce inscrite à l’Annexe II de la CITES et classée Vulnérable par l’UICN.
3.2. Répartition par habitat et usages ethnobotaniques
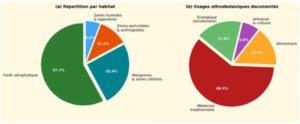
La répartition spatiale des espèces révèle une nette différenciation entre les habitats (Figure 4a). Les forêts xérophytiques, couvrant environ 57,7 % de la superficie inventoriée, abritent la majorité de la diversité floristique (41 espèces). Les mangroves et zones côtières hébergent 18 espèces (25,4 %), avec une forte spécialisation écologique. Les analyses ethnobotaniques (Figure 4b) montrent que 60,4 % des espèces sont utilisées en médecine traditionnelle, 15,4 % à des fins alimentaires, et 6,6 % à des fins artisanales ou culturelles.
3.3. Espèces d’intérêt pour la conservation
Parmi les espèces recensées, plusieurs présentent un intérêt patrimonial majeur (Figure 5). Guaiacum officinale (Zygophyllaceae), inscrit à l’Annexe II de la CITES et classé Vulnérable par l’UICN, a été identifié dans les zones de forêt sèche. Zamia rosea (Zamiaceae), cycadale rare et endémique d’Hispaniola, a également été documentée. Deux endémiques ont été recensées : Allophylus haitiensis (Sapindaceae) et Malpighia hispaniolica (Malpighiaceae). Swietenia mahagoni (Meliaceae), classé Vulnérable par l’UICN, a également été noté, soumis à la coupe sélective pour son bois précieux.
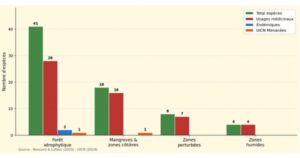
Tableau 2. Espèces à fort intérêt pour la conservation au PNN-LdH.
| Espèce | Famille | Statut UICN | Endém. | Usage principal | Menace |
| Guaiacum officinale | Zygophyllaceae | VU / CITES II | Caribbean | Anti-inflammatoire | Surexploitation |
| Allophylus haitiensis | Sapindaceae | Non évalué | Hispaniola | Alimentaire | Forestry |
| Zamia rosea | Zamiaceae | Non évalué | Hispaniola | Pharmacol. | Rareté, collecte |
| Swietenia mahagoni | Meliaceae | VU | Caribbean | Bois précieux | Coupe sélective |
| Rhizophora mangle | Rhizophoraceae | LC | Pantropical | Prot. côtière | Coupes charbon |
| Avicennia germinans | Acanthaceae | LC | Pantropical | Prot. côtière | Dégrad. côtière |
3.4. Herbier de référence
L’ensemble des 71 espèces a fait l’objet d’une collecte, d’un pressage, d’un séchage et d’un montage selon les standards internationaux de l’herborisation. Chaque planche est associée à une fiche normalisée comprenant 16 champs d’information. Cet herbier, hébergé au bureau de Helvtas à Belle-Anse, constitue le premier outil de référence botanique systématique pour le PNN-LdH.
4. Discussion
4.1. Structure floristique et contexte biogéographique
La prédominance des Fabaceae (14,1 %) est cohérente avec la littérature sur les forêts sèches néotropicales, où cette famille occupe généralement une position dominante en raison de son rôle dans la fixation de l’azote atmosphérique (Cano-Ortiz et al., 2016). La diversité des Lamiaceae, Cactaceae et Apocynaceae confirme le caractère xérophytique des formations, ces familles étant caractéristiques des milieux semi-arides tropicaux. Avec 71 espèces dans 30 familles, la richesse floristique apparaît modérée mais significative, compte tenu des limites méthodologiques et du caractère semi-aride du milieu.
4.2. Rôles écologiques des espèces recensées
Les mangroves (Laguncularia racemosa, Rhizophora mangle, Avicennia germinans) jouent un rôle fondamental dans la protection côtière et la fonction de nurserie pour les espèces marines. Ward et al. (2016) ont démontré que ces formations réduisent l’énergie des vagues de 50 à 70 % et séquestrent 3 à 5 fois plus de carbone par hectare que les forêts tropicales humides. Ellison (2015) a développé un cadre méthodologique pour l’évaluation de la vulnérabilité des mangroves, applicable au PNN-LdH. La présence de Prosopis juliflora, espèce potentiellement envahissante, nécessite cependant un suivi rigoureux (Hilaire, 2014).
4.3. Importance ethnobotanique et pharmacologique
Avec 77 % des espèces présentant des usages médicinaux documentés, le PNN-LdH représente une pharmacopée végétale de premier ordre. Ces résultats corroborent les travaux de Salla (2015) et de Vardeman et al. (2014) sur l’utilisation des plantes médicinales par les communautés haïtiennes. Parmi les espèces les plus remarquables, Phyllanthus amarus (hépatoprotecteur), Guaiacum officinale (anti-inflammatoire, UICN VU), Annona muricata (propriétés anticanceréreuses étudiées) et Psidium guajava (anti-diarrhéique, validé par le programme TRAMIL) méritent une attention particulière. McKee (2004) rappelle que les connaissances traditionnelles sur les usages des plantes représentent un patrimoine immatériel menacé de disparition. L’herbier institutionnel constitue un outil précieux pour la double conservation de ce patrimoine – biologique et culturel.
4.4. Menaces sur la biodiversité et implications pour la conservation
Les principales menaces identifiées sont : (1) la déforestation et la coupe de mangroves pour le charbon de bois ; (2) l’érosion côtière et l’envasement des lagunes ; (3) le pâturage caprin non contrôlé ; (4) le changement climatique, avec des projections de réduction des précipitations et de montée du niveau de la mer de 0,5 m d’ici 2100, affectant 23 % des mangroves caraïbéennes (Wilson, 2017). L’UNEP (2020) rapporte que les mangroves haïtiennes diminuent à un rythme d’environ 1 % par an, soulignant l’urgence d’une gestion fondée sur des données scientifiques actualisées. La présence de Guaiacum officinale (CITES II, UICN VU), de Swietenia mahagoni (UICN VU) et de deux endémiques d’Hispaniola renforce la justification du statut d’aire protégée et souligne l’urgence de mesures de conservation ciblées.
4.5. L’herbier comme outil de conservation et de recherche
Davis et al. (2023) soulignent que les herbaria modernes sont capables de fournir des données de référence pour la surveillance à long terme des écosystèmes, en intégrant des données moléculaires, chimiques et morphologiques. La perspective de numérisation et de mise en ligne des spécimens sur des plateformes internationales (GBIF, JSTOR Global Plants) maximiserait considérablement la valeur scientifique de cette collection. L’implication des communautés locales dans le processus constitue une démarche participative prometteuse, contribuant au renforcement des capacités locales et à la sensibilisation à la biodiversité, dans l’esprit des principes d’Ostrom (1990) pour la gestion durable des biens communs.
5. Conclusion
Cette étude présente le premier inventaire floristique systématique du PNN-LdH, assorti de la création d’un herbier institutionnel de référence. Avec 71 espèces vasculaires dans 30 familles, dont des endémiques d’Hispaniola et des espèces menacées (UICN, CITES), les résultats confirment la haute valeur patrimoniale de cette aire protégée. Le fort taux d’espèces à usages médicinaux (77 %) souligne l’imbrication entre conservation biologique et patrimoine culturel.
Les perspectives prioritaires incluent : (à court terme) la numérisation de l’herbier sur GBIF et JSTOR Global Plants, l’extension de l’inventaire aux zones sous-échantillonnées et la mise en place de transects permanents ; (à moyen terme) le suivi phénologique des espèces clés, les analyses moléculaires (ADN code-barre) sur les endémiques et l’intégration des données dans un SIG couplé à la télédétection (Hong et al., 2025) ; (à long terme) le développement de filières économiques durables (produits forestiers non ligneux certifiés, écotourisme) et le renforcement de la gouvernance locale. Ces recommandations s’inscrivent dans les engagements d’Haïti au titre des ODD 14 et 15 et du Cadre de Kunming-Montréal (30 % d’aires protégées d’ici 2030).
Remerciements
Cette étude a été réalisée dans le cadre du Projet INOVEE, financé par HELVETAS Haïti (Fonds Européen de Développement, réf. EuropeAid/178173/ID/ACT/HT). Les auteurs remercient Dérisier Jean-Louis (Directeur du PNN-LdH), Alix Bazil et Feguens Joseph (collecteurs).
References
Alain, H. (1953–1979). Flora de Cuba (5 volumes). Contribuciones Ocasionales del Museo de Historia Natural del Colegio De La Salle, La Habana.
BUCOSEH. (s.d.). Rapport d’étude : Évaluation écologique rapide des formations végétales du PNN-LdH.
Cano-Ortiz, A., Musarella, C. M., Piñar Fuentes, J. C., Pinto Gomes, C. J. & Cano, E. (2016). Distribution patterns of endemic flora to define hotspots on Hispaniola. Systematics and Biodiversity, 14(3), 261–275. https://doi.org/10.1080/14772000.2015.1135195
Ceballos, G., Ehrlich, P. R. & Dirzo, R. (2017). Biological annihilation via the ongoing sixth mass extinction signaled by vertebrate population losses and declines. PNAS, 114(30), E6089–E6096. https://doi.org/10.1073/pnas.1704949114
Céliscar, A. (2017). Étude des variations climatiques dans la région du Sud-Est d’Haïti. Rapport BUCOSEH.
Davis, C. C., Willis, C. G., Connolly, B., Kelly, T. & Ellison, A. M. (2023). The herbarium of the future. Trends in Ecology & Evolution, 38(5), 412–423. https://doi.org/10.1016/j.tree.2022.11.015
Ellison, J. C. (2015). Vulnerability assessment of mangroves to climate change and sea-level rise impacts. Wetlands Ecology and Management, 23(2), 115–137. https://doi.org/10.1007/s11273-014-9397-8
FAO. (2010). Global Forest Resources Assessment 2010. Food and Agriculture Organization of the United Nations.
Forbes, D. (2013). Caribbean ecotourism and biodiversity conservation. Journal of Ecotourism, 12(1), 34–50.
Haiti Biodiversity. (2023). Haiti Biodiversity and Nature Conservation. BioDB. https://biodb.com/region/haiti
Haiti National Trust. (2023). Research & Science. https://haititrust.org/research-science
HELVETAS Haïti. (2025). La restauration des récifs coralliens au parc Lagon des Huîtres.
Hilaire, J. V. (2014). Évaluation écologique des aires protégées et des zones tampons du département du Sud-Est.
Hong, F., Ward, R. D. & James, C. M. (2025). Decoding primary forest changes in Haiti and the Dominican Republic using Landsat time series. Remote Sensing of Environment, 290, 113456. https://doi.org/10.1016/j.rse.2024.113456
Lang, P. L. M., Willems, F. M., Scheepens, J. F., Burbano, H. A. & Bossdorf, O. (2018). Using herbaria to study global environmental change. New Phytologist, 221(1), 110–121. https://doi.org/10.1111/nph.15401
Liogier, A. H. (1982–2000). La flora de la Española (9 volumes). Universidad Central del Este, San Pedro de Macorís.
Liogier, A. H. (2000). Diccionario botánico de nombres vulgares de La Española (2e éd.). Jardín Botánico Nacional, Santo Domingo.
McKee, K. L. (2004). Global change impacts on mangrove ecosystems. USGS Fact Sheet.
Meineke, E. K., Davis, C. C. & Davies, T. J. (2018). The unrealized potential of herbaria for global change biology. Ecological Monographs, 88(4), 505–525. https://doi.org/10.1002/ecm.1307
Ministère de l’Environnement (MDE). (2015). Programme Aligné d’Action National de Lutte contre la Désertification.
Myers, N., Mittermeier, R. A., Mittermeier, C. G., da Fonseca, G. A. B. & Kent, J. (2000). Biodiversity hotspots for conservation priorities. Nature, 403, 853–858. https://doi.org/10.1038/35002501
Nagelkerken, I. et al. (2008). The habitat function of mangroves for offshore fish and invertebrate populations. Estuarine, Coastal and Shelf Science, 74(3), 155–162.
Navarro, N. (2019). Community perceptions of tourism impacts on coastal protected areas. Journal of Marine Science and Engineering, 7(8), 274.
Noncent, D., Lafleur, P.N. (2025). Rapport scientifique – Inventaire de la biodiversité végétale et création d’un herbier au sein du Parc National Naturel Lagon des Huîtres (PNN-LdH), Belle-Anse (Sud-Est, Haïti). Rapport produit dans le cadre du Projet INOVEE de HELVETAS, AHAAMES, UniQ, avec l’appui scientifique de l’ERC2/UniQ, financé par le Fonds Européen de Développement. Référence : EuropeAid/178173/ID/ACT/HT
Ostrom, E. (1990). Governing the Commons: The Evolution of Institutions for Collective Action. Cambridge University Press.
Salla, B. (2015). Prise en charge des symptômes douloureux par la médecine traditionnelle haïtienne. Douleurs Sans Frontières, FOKAL, Port-au-Prince.
TNC. (2019). Rapport de la ligne de base pour la caractérisation, l’inventaire et l’analyse des ressources biologiques du PNN-LdH.
TRAMIL. (1995–présent). Programme de recherche appliquée à l’usage populaire de plantes médicinales dans la Caraïbe. www.tramil.net
Tropicos. Missouri Botanical Garden. http://www.tropicos.org
UNEP-WCMC. (2020). Protected Planet Report 2020. UN Environment Programme.
UNEP. (2020). Mangrove restoration in Haiti moves up a gear. United Nations Environment Programme.
Vardeman, E. T., Kennelly, E. J. & Vandebroek, I. (2014). Haitian women in New York City use global food plants for women’s health. Economic Botany, 68(3), 247–270.
Ward, R. D., Friess, D. A., Day, R. H. & Mackenzie, R. A. (2016). Impacts of climate change on mangrove ecosystems: a region by region overview. Ecosystem Health and Sustainability, 2(4), e01211. https://doi.org/10.1002/ehs2.1211
Wilson, R. (2017). Impacts of Climate Change on Mangrove Ecosystems in the Coastal and Marine Environments of Caribbean SIDS. Caribbean Regional Fisheries Mechanism.
noncent-et-lafleur-2026.-inventaire-floristique-et-creation-dun-herbier-de-reference-pnn-ldh-3.docx